DGZ-Newsletter 02 | 2026
Im DGZ-Newsletter werden wissenschaftliche Informationen zur Zahnerhaltung kompakt und verständlich auf den Punkt gebracht. Die Inhalte werden von Expertinnen und Experten der deutschen Universitätszahnkliniken verfasst, die exklusiv von interessanten Entwicklungen aus ihrer aktuellen Forschungsarbeit berichten.
Im zweiten Newsletter dieses Jahres berichtet PD Dr. Konstantin Scholz aus Freiburg unter Neues aus der Forschung über Studien zu Lanthanoidsalzen mit vielversprechendem Potenzial als Kariostatika. Für eine klinische Anwendung sind jedoch weitere Untersuchungen zu Stabilität und Wirkung erforderlich. Im Expertengespräch beleuchtet Dr. Scholz die Anforderungen und Wirkungsweisen von Kariostatika sowie die methodischen Herausforderungen und die Übertragung von in-vitro- auf in-vivo-Bedingungen im Kontext der modernen Prophylaxe in der Zahnmedizin.
Tipps für die Praxis gibt Prof. Dr. Sebastian Paris aus Berlin zur Anwendung von Silberdiaminfluorid (SDF) als noninvasive, evidenzbasierte Therapieoption für kariöse Läsionen. Hinweise für eine rechtssichere Abrechnung bei einer Therapie mit SDF gibt Emine Parlak von der Charité Berlin.
Lanthanoidsalze als neuartige Kariostatika?
Lanthanoidsalze könnten anhand aktueller in vitro-Daten günstige Eigenschaften für einen potenziellen Einsatz als Kariostatikum haben. In der Theorie wäre hier eine Einlagerung in das Kristallgitter des Hydroxylapatits verglichen mit etablierten Fluoriden möglich, jedoch nicht an die Stellen der Hydroxid-, sondern der Kalziumionen. Für den Einsatz als präventive Substanz ist hierfür zunächst eine Akkumulation auf der Zahnhartsubstanz eine Grundvoraussetzung.
In einer Studie zu Cer- und Samariumnitraten zeigte sich, dass diese Salze nach kurzer Applikationszeit von 30 Sekunden auf humanem Schmelz in vitro mittels energiedispersiver Röntgenmikrobereichsnalaytik detektierbare Auflagerungen bilden können – sowohl auf poliertem Schmelz als auch in Gegenwart einer Speichelpellikel. Nach Präparation mittels Focused-Ion-Beam konnte mittels Transmissionselektronenmikroskopie auch dargestellt werden, dass die netz- und kugelförmigen Präzipitate Interaktionen in den gesunden Zahnschmelz bis zu einer Tiefe von einigen hundert Nanometern zeigten (Abb. 1).
 Abb. 1: Samarium-haltige Präzipitate auf Zahnschmelz mit netzartiger Struktur und Interaktion unterhalb der Oberfläche (weißer Kreis). Bildquelle: https://pmc.ncbi.nlm.nih.gov/articles/PMC11425791/.
Abb. 1: Samarium-haltige Präzipitate auf Zahnschmelz mit netzartiger Struktur und Interaktion unterhalb der Oberfläche (weißer Kreis). Bildquelle: https://pmc.ncbi.nlm.nih.gov/articles/PMC11425791/.
Eine zweite Arbeit untersuchte die Interaktion derselben Lanthanoidsalze mit humanem Dentin. Hier wurden Dentinproben mit und ohne Schmierschicht eingesetzt. Diese Schmierschicht, die bei mechanischer Bearbeitung der Dentinoberfläche entsteht, beispielsweise durch Präparation, kann die Anlagerung und gegebenenfalls oberflächennahe Penetration in Dentin beeinflussen. Sowohl mit als auch ohne Schmierschicht war hierbei eine deutliche oberflächliche Präzipitation detektierbar. Diese Präzipitationen zeigten sich in den Proben ohne Schmierschicht vorwiegend im Bereich der Dentintubuli (Abb. 2).
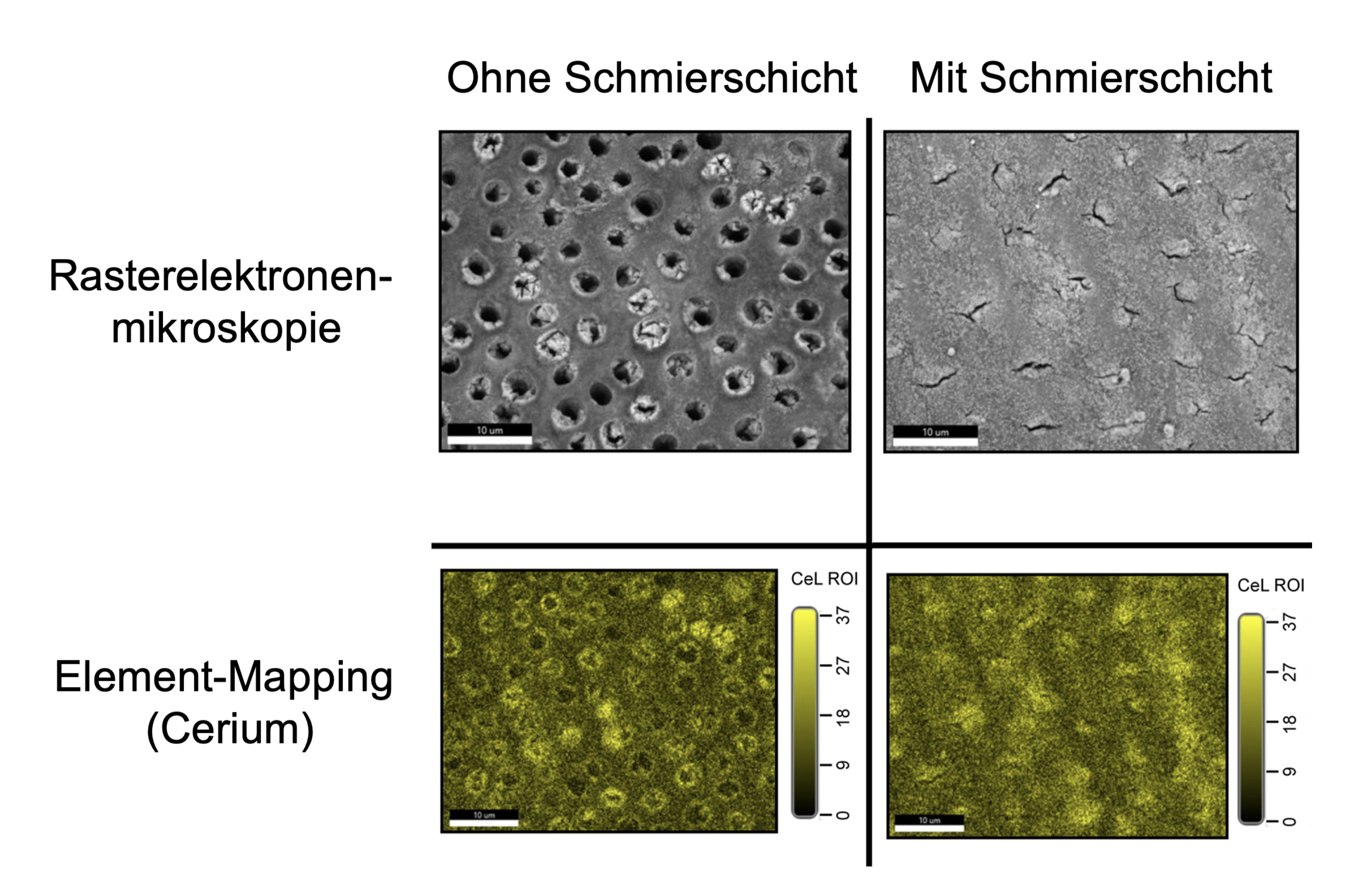 Abb. 2: Sichtbare Oberflächliche Cerium-Präzipitation (gelb markiert), vorwiegend im Bereich der Dentintubuli. Bildquelle: https://www.sciencedirect.com/science/article/abs/pii/S0003996924001742?via%3Dihub
Abb. 2: Sichtbare Oberflächliche Cerium-Präzipitation (gelb markiert), vorwiegend im Bereich der Dentintubuli. Bildquelle: https://www.sciencedirect.com/science/article/abs/pii/S0003996924001742?via%3Dihub
Die beiden Studien konnten zeigen, dass Lanthanoidnitrate Grundvoraussetzungen für die Interaktion mit Zahnhartsubstanzen aufweisen. Weitere Studien müssen die Stabilität dieser Präzipitate sowie den Einfluss auf Parameter wie Oberflächenhärte, Säreresistenz und Mineralgehalt intakter und demineralisierter Zahnhartsubstanzen durch die Applikation beeinflusst werden.
Autor: Priv.-Doz. Dr. Konstantin Scholz, geschäftsführender Oberarzt der Klinik für Zahnerhaltungskunde und Parodontologie des Universitätsklinikums Freiburg
Moderne Kariesprophylaxe: Potenziale und Grenzen von Kariostatika
Interview mit Priv.-Doz. Dr. Konstantin Scholz, geschäftsführender Oberarzt der Klinik für Zahnerhaltungskunde und Parodontologie des Universitätsklinikums Freiburg (Foto: privat)
Prophylaktische Herangehensweisen nehmen heutzutage einen hohen Stellenwert in der zahnmedizinischen Versorgung ein. Priv.-Doz. Dr. Konstantin Scholz beleuchtet die Anforderungen und Wirkungsweisen von Kariostatika, während er dabei auf die methodischen Herausforderungen bei der Untersuchung derartiger Substanzen und die Hürde der Übertragung von in-vitro auf in-vivo Umgebungsbedingungen eingeht.
)
Herr Dr. Scholz, Wie definieren Sie Kariostatika?
Kariostatika haben zum Ziel, Karies zum Stillstand zu bringen oder im Idealfall sogar Remineralisation von Zahnhartsubstanz in bereits bestehenden Läsionen zu fördern. Eine ideale Substanz sollte hierbei biokompatibel sein und sowohl mit demineralisierter, als auch intakter Zahnhartsubstanz interagieren können, und zumindest nicht zu mehr Akkumulation von Bakterien auf der Oberfläche führen. Dafür sind alle genannten Punkte relevant – zunächst muss natürlich eine Interaktion oder Penetration der Pellikel stattfinden, die bei Kontakt von Dentin und Schmelz mit Speichel unmittelbar entsteht.
In welchem Umfang lassen sich die Wirkmechanismen von Kariostatika erklären, und welche Aspekte gelten noch als unzureichend erforscht?
Hinsichtlich der Mechanismen können Substanzen zum einen in poröse Zahnhartsubstanz eindringen, aber auch an der Oberfläche als Ionenreservoir oder sogenannte Opferschicht ausfallen, die dann über den Tag statt der Zahnhartsubstanz selbst den wechselnden pH-Werten ausgesetzt ist. Da im Laufe des Lebens und selbst im Laufe des Tages die Mundhöhle von Menschen mit zahlreichen verschiedenen Substanzen in Kontakt kommt, ist die Abstimmung dieser Mechanismen bedeutend, da eine zu ausgeprägte oberflächliche Auflagerung natürlich auch die Tiefenwirkung beeinflusst.
Welche Unterschiede bestehen zwischen Fluoridpräparaten und Wirkstoffen wie Hydroxylapatit, CPP-ACP oder Peptiden hinsichtlich ihrer Interaktion mit Zahnhartsubstanzen?
Bei Fluoriden als Substanzklasse mit der mit großem Abstand meisten Evidenz wird neben der Kalziumfluorid-Deckschicht, die vor allem bei höherkonzentrierten Präparaten mit saurem pH-Wert auftritt, auch eine Modifikation des Kristallgitters von Hydroxylapatit angestrebt. Durch Einlagerung von Fluorid an die Stelle des Hydroxid-Ions entstehen höhere Gitterspannungen und eine geringere Säurelöslichkeit. Peptidbasierte Kariostatika sollen die Vorgänge der de-novo-Amelogenese imitieren, indem selbst-organisierende Peptide Kalziumionen um sich lagern sollen, die dann zur Remineralisation beitragen. Es gibt hierzu jedoch bislang keine klinischen Daten und es ist fraglich, inwieweit diese Peptide in vitro auf der Oberfläche akkumulieren oder gar in die Tiefe von Porositäten gelangen und ihre Wirkung entfalten können. Kariostatika auf Basis von Kalziumphosphatverbindungen, wie z.B. Nanohydroxylapatit oder CPP-ACP, verfolgen eher die oben beschriebene Strategie der Bildung einer Opferschicht, die während Phasen überwiegender Demineralisation die Zahnhartsubstanz schützen sollen.
Welche methodischen Herausforderungen bestehen bei der Übertragung von in-vitro-Ergebnissen zu Kariostatika?
Klinisch entstehen kariöse Läsionen aus einem länger anhaltenden Ungleichgewicht im Mikrobiom in Richtung einer Dysbiose und einer Netto-Demineralisation, was die Prozesse komplex und multifaktoriell macht. Der pH-Wert kariostatischer Substanzen beeinflusst dabei stark die Interaktion mit der Zahnhartsubstanz und die Speichelzusammensetzung und -menge ist ebenfalls hoch relevant für die Wirkung. Eine Modulation des Biofilms in Richtung der Eubiose wäre wünschenswert, zumindest ein Shift in Richtung Dysbiose sollte aber nicht stattfinden. Innerhalb der Biofilme selbst können Konzentrationsgradienten der aufgetragenen Substanzen auftreten. All diese Aspekte können nur schwer in ein einziges in-vitro-Modell integriert werden, weshalb translationale Ansätze unter Einbeziehung von Grundlagenforschung und klinischen Studien notwendig sind.
Herr Dr. Scholz, vielen Dank für das Gespräch.
Das Interview führten Priv.-Doz. Dr. Julia Lubauer und Dr. Sabina Würsching
Silberdiaminfluorid im Kariesmanagement
von Prof. Dr. Sebastian Paris, Direktor der Abteilung für Zahnerhaltung, Präventiv- und Kinderzahnmedizin in der Charité Universitätsmedizin Berlin. Foto: Sebastian Paris
Silberdiaminfluorid (SDF) verbindet die jahrzehntelang bekannte antimikrobielle Wirkung von Silberionen mit der remineralisierenden Wirkung von Fluorid – und bietet damit eine noninvasive und evidenzbasierte Therapieoption für kariöse Läsionen.
Bereits im 19. Jahrhundert wurden silberhaltige Lösungen wie Silbernitrat wegen ihrer antimikrobiellen Wirkung in der Zahnmedizin eingesetzt. Auch Amalgam verdankte dem darin enthaltenen Silber seine antibakterielle und Sekundärkaries-hemmende Wirkung.
)
Silberdiaminfluorid (SDF) wurde in Japan entwickelt und fand dort zuerst eine weite Verbreitung als Karies-arretierendes Medikament. SDF ist eine wässrige Lösung, die sowohl hochkonzentrierte Silber- (ca. 25%) als auch Fluoridionen (ca. 5%) enthält. Die Silberionen wirken stark antimikrobiell, indem sie Bakterienmembranen schädigen und Enzyme hemmen, während die Fluoridionen primär auf die Mineralisation wirken, indem sie die Remineralisation fördern und eine Demineralisation hemmen.
Während SDF in vielen Ländern Asiens, Südamerikas und Australien schon seit Jahrzehnten erfolgreich zur Karieskontrolle eingesetzt wird, verlief die Zulassung und damit auch die zahnärztliche Anwendung in Europa und Nordamerika schleppend. In den USA erhielt SDF erst 2014 die FDA-Zulassung, zunächst zur Behandlung von Dentinhypersensibilität, bevor 2016 die Indikation auf die Kariesarretierung erweitert wurde.1 In Europa und Deutschland ist SDF (Riva Star® und Riva Star Aqua®, SDI Limited) bis heute nur als Medizinprodukt für die Behandlung von Zahn-Überempfindlichkeiten zugelassen. Daher erfolgt die Behandlung von Karies mit SDF in Deutschland noch immer „off-label“.
Indikation
Mit SDF kann eine Arretierung kariöser Läsionen erreicht werden, selbst wenn andere ätiologische Faktoren, wie Mundhygiene und Ernährung nicht optimal kontrolliert werden können. Daher bietet sich SDF vor allem bei Patienten an, bei denen andere präventive Maßnahmen an ihre Grenzen stoßen und für die eine restaurative Therapie nicht, oder nur eingeschränkt in Frage kommt. So wird SDF historisch besonders in der Kinderzahnheilkunde, zum Beispiel bei Frühkindlicher Karies (ECC) und bei Vorschulkindern angewendet. Auch bei Patienten mit Behinderungen und Patienten mit Zahnarztphobie ist SDF ein verbreitetes Mittel zur Kariesarretierung. In den vergangenen Jahren findet SDF aber auch in Alterszahnheilkunde eine immer weitere Verbreitung.2
Die Wirksamkeit der Arretierung von Karies durch SDF ist sowohl für die Kinderzahnheilkunde3 als auch für Wurzelkaries4 inzwischen gut wissenschaftlich belegt.
Anwendung
Insbesondere wegen der off-label-Indikation bei der Arretierung von Karies sollten die Patienten bzw. deren Sorgeberechtigte vor der Anwendung über Risiken und Nebenwirkungen aufgeklärt und dies gut dokumentiert werden. Die häufigste Nebenwirkung ist hierbei die Schwarzfärbung der behandelten Läsionen. Durch die Reduktion der Silberionen kommt es einige Zeit nach der Anwendung zur Bildung elementaren Silbers im behandelten Dentin, welches sich dadurch schwarz verfärbt. Insbesondere bei sichtbaren Läsionen wie bei der ECC führt dies dazu, dass die vormals gelblich braunen Läsionen tiefschwarz werden und nun auch für Laien auffällig sind. Während dieser Effekt in der Kinderzahnheilkunde oftmals von den Eltern der Patienten als kritisch empfunden wird, spielen dagegen die Verfärbungen in der Alterszahnheilkunde kaum eine Rolle, da die Wurzelkaries zumeist nicht in einsehbaren Bereichen lokalisiert ist.
Die klinische Anwendung von SDF ist relativ einfach. Die Läsion wird vom Biofilm gereinigt und getrocknet (Abb. 1), ggf. kann das umliegende Weichgewebe wird mit Vaseline vor Kontaminationen geschützt werden. Auch sollte die Kleidung des Patienten und des Personals wie auch die zahnärztliche Einheit unbedingt vor Kontakt mit der Lösung schützt werden – etwaige Spritzer und Flecken färben sich schwarz und lassen sich zumeist nicht mehr entfernen. Nun wird das SDF mit einem Microbrush-Applikator für 30–60 Sekunden auf die Läsion aufgetragen (Abb. 2) und anschließend leicht verblasen. Eine Wiederholung nach 6 bis 12 Monaten wird empfohlen, um den Arretierungseffekt aufrechtzuerhalten (Abb. 3). Wie bei allen kariesarretierenden Ansätzen, sollte der Erfolg der Behandlung kontrolliert werden. Dabei richtet sich das Recall-Intervall nach dem Kariesrisiko des jeweiligen Patienten.
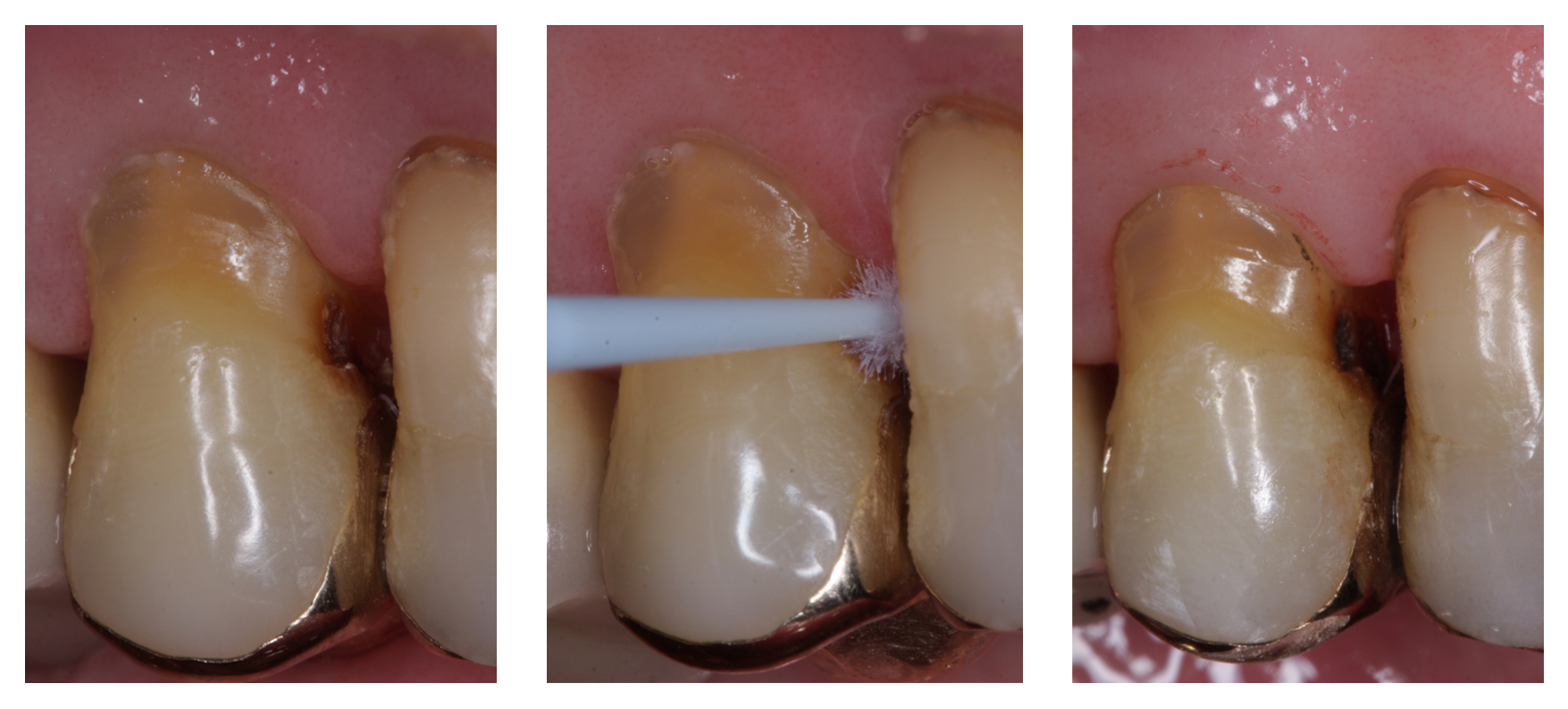 Abb. 1: Aktive approximale Wurzelkaries mit oberflächlicher Kavitation; Abb. 2: Applikation von SDF mittels Microbrush; Abb. 3: Läsion nach 6 Wochen. Die Läsion ist arretiert und schwarz gefärbt. Fotos: Sebastian Paris
Abb. 1: Aktive approximale Wurzelkaries mit oberflächlicher Kavitation; Abb. 2: Applikation von SDF mittels Microbrush; Abb. 3: Läsion nach 6 Wochen. Die Läsion ist arretiert und schwarz gefärbt. Fotos: Sebastian Paris
Zusammenfassend lässt sich sagen, dass SDF ein wertvolles Medizinprodukt zur Karieskontrolle ist, das insbesondere bei Patientengruppen seine Anwendung findet, bei denen präventive und restaurative Maßnahmen an ihre Grenzen stoßen.
Gao S. S., Amarquaye G., Arrow P., Bansal K., Bedi R., Campus G., et al. Global Oral Health Policies and Guidelines: Using Silver Diamine Fluoride for Caries Control. Front Oral Health. 2021;2:685557, DOI: 10.3389/froh.2021.685557.
Grandjean M. L., Maccarone N. R., McKenna G., Muller F., Srinivasan M. Silver Diamine Fluoride (SDF) in the management of root caries in elders: a systematic review and meta-analysis. Swiss Dent J. 2021;131(5):417-24, DOI: 10.61872/sdj-2021-05-02.
Gao S. S., Zhao I. S., Hiraishi N., Duangthip D., Mei M. L., Lo E. C. M., et al. Clinical Trials of Silver Diamine Fluoride in Arresting Caries among Children: A Systematic Review. JDR Clin Trans Res. 2016;1(3):201-10, DOI: 10.1177/2380084416661474.
Oliveira B. H., Cunha-Cruz J., Rajendra A., Niederman R. Controlling caries in exposed root surfaces with silver diamine fluoride: A systematic review with meta-analysis. J Am Dent Assoc. 2018;149(8):671-9 e1, DOI: 10.1016/j.adaj.2018.03.028.
SDF-Abrechnung: So setzen Sie Silberdiaminfluorid rechtssicher um
von Emine Parlak, Stabsstelle Kosten- und Erlösmanagement, Charité Universitätsmedizin Berlin I Centrum 3 für Zahn-, Mund- und Kieferheilkunde (Foto: Emine Parlak).
Für Silberdiaminfluorid (SDF) existiert weder in der GOZ noch im BEMA eine eigene Gebührenziffer. Die Abrechnung erfolgt daher grundsätzlich analog nach § 6 Abs. 1 GOZ. Entscheidend ist dabei immer die konkrete Indikation: Wird SDF zur Kariesarretierung, zur Desensibilisierung oder als oberflächliche therapeutische Maßnahme eingesetzt, muss die Analogposition entsprechend gewählt werden.
Maßgeblich sind wie üblich Art der Leistung, Zeitaufwand, Schwierigkeitsgrad und Materialeinsatz – eine pauschale „Standardziffer“ für SDF gibt es nicht. Das heißt: Nicht jede SDF-Anwendung braucht dieselbe Analogie — der Zweck der Behandlung ist entscheidend.
)
Wichtig ist auch die klare Abgrenzung zu bestehenden Leistungen: Die GOZ 1020 (Fluoridierung) ist für SDF nicht geeignet, da Wirkung und therapeutischer Anspruch deutlich darüber hinausgehen. Auch im BEMA findet sich keine entsprechende Position. Bei gesetzlich Versicherten kann die Diagnostik zwar weiterhin über den BEMA erfolgen, die SDF-Anwendung selbst stellt jedoch in der Regel eine private Leistung dar und muss vorab entsprechend vereinbart werden.
Für die praktische Umsetzung empfiehlt sich ein strukturierter Ablauf:
Nach Festlegung der Indikation sollte die Leistung detailliert dokumentiert und anschließend eine passende Analogposition ausgewählt werden.
Die Materialkosten werden in der Regel in die Analogleistung eingerechnet, können jedoch bei besonderem Aufwand entsprechend berücksichtigt werden.
Bei GKV-Patienten ist zudem vorab eine schriftliche Privatvereinbarung erforderlich.
Was zusätzlich abrechenbar sein kann:
Zusätzlich zur SDF-Hauptleistung können je nach tatsächlichem Ablauf weitere Leistungen separat ansetzbar sein, wenn sie nicht bereits in der Analogposition enthalten sind. Dazu gehören typischerweise:
Beratung/Untersuchung: GOZ 0010, GOÄ1 oder ggf. BEMA 01-entsprechend, wenn GKV-Konstellation vorliegt.
Zuschlag für Kinder bis zum vollendeten 4 Lebensjahr: GOZ K1
Aufstellung eines schriftlichen Heil- und Kostenplans: GOZ 0030
Vitalitätsprobe GOZ: 0070
Oberflächenanästhesie: 0080Entfernung harter und weicher Zahnbeläge: GOZ 4050/4055
Begleitleistungen wie Trockenlegung oder Isolation: GOZ 2040 oder 2030 sofern sie abrechnungsrechtlich selbstständig sind.
Weitere konservierende Maßnahmen, wenn sie zusätzlich durchgeführt wurden.
Die genannten zusätzlich abrechenbaren Leistungen sind nicht als abschließend oder rechtlich verbindlich zu verstehen; die Abrechnungsfähigkeit ist jeweils im Einzelfall nach GOZ/GKV‑Vorgaben und individueller Behandlungsdokumentation zu prüfen
Fazit: SDF ist abrechnungstechnisch kein Standardfall, sondern erfordert immer eine individuelle Bewertung. Eine klare Dokumentation, eine schlüssige Begründung und ein einheitliches Vorgehen im Team sorgen dafür, dass die Abrechnung nachvollziehbar und rechtssicher bleibt.